刚刚,康诺亚生物成功登陆港交所
继先声药业后,国内又迎来了一家同时研发自免及肿瘤领域新药的上市企业。
据了解,康诺亚今年2月10日宣布完成1.3亿美元C轮融资,4月9日向港交所递交招股书,今日(7月8日)成功上市,可以说一气呵成,同为高瓴资本投资企业,跟之前的嘉和生物、云顶新耀IPO之路有着异曲同工之妙。
康诺亚于2016年成立,专注于自主发现及开发自体免疫及肿瘤治疗领域的创新生物疗法,并基于其创新抗体发现平台及自有新型T细胞重定向1(nTCE)双特异性抗体平台的技术,目前已开发出包括3款自身免疫治疗产品和6款肿瘤治疗产品,且5款为临床阶段候选药物,3款处于可进入临床试验申请阶段。
据统计,自身免疫领域存在100多种疾病类型且病患群体庞大,近年来,修美乐亦一直以药王的称号霸占全球最畅销药品榜首位置,且2020年销售数据显示,自免及炎症药物位列第二,仅次于肿瘤。随着艾伯维、礼来、辉瑞、诺华、恒瑞、先声药业等药企争相布局,自免或将成为继肿瘤之后的又一活跃赛道。
此次IPO后,康诺亚表示所筹款项将主要用于核心及主要产品的研发及商业化、其他在研产品的临床前评估及临床开发。
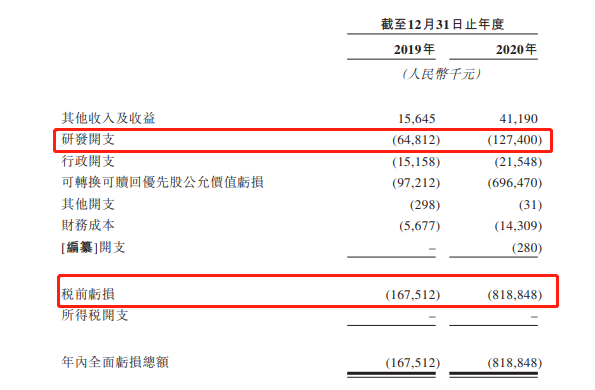
截图自招股书
虽已亏损10亿,但此次IPO康诺亚引进国际长线基金UBSAM、Invesco、Temasek,专业医疗投资者Hudson Bay、Janchor、Springhill、Octagon、Sage,及高瓴资本、博裕资本、联想之星在内的老股东等15名基石投资者,共认购1.9亿美元,占比超48%。康诺亚为什么获得如此多的资本青睐呢?
首先,康诺亚有着经验丰富的管理团队,创始人陈博博士曾先后参与创立武汉华鑫康源生物医药有限公司、君实生物2家生物医药企业,并曾领导中国首个获批的国产PD-1抗体特瑞普利单抗的开发工作。另外一名创始人王常玉博士拥有超23年的生物医药研发经验,曾担任辉瑞癌症免疫总监,也曾领导全球首款PD-1抗体Nivolumab的开发。
临床进展方面,康诺亚的5款临床阶段候选药物在国产同靶点药物或同类别药物中处于取得中国及美国临床试验申请批准的前3位,且优先布局自身免疫领域。此外,为配合研发工作,康诺亚已与石药集团、乐普生物、天广实及诺诚健华达成合作以开发及商业化其候选药物。
同时为满足商业化需求,康诺亚已在成都建成首个符合现行药品生产质量规范的生产设施,总产能为1600公升。并预计在2022年完成第一阶段新商业化规模生产设施,可提供16000公升的额外产能。
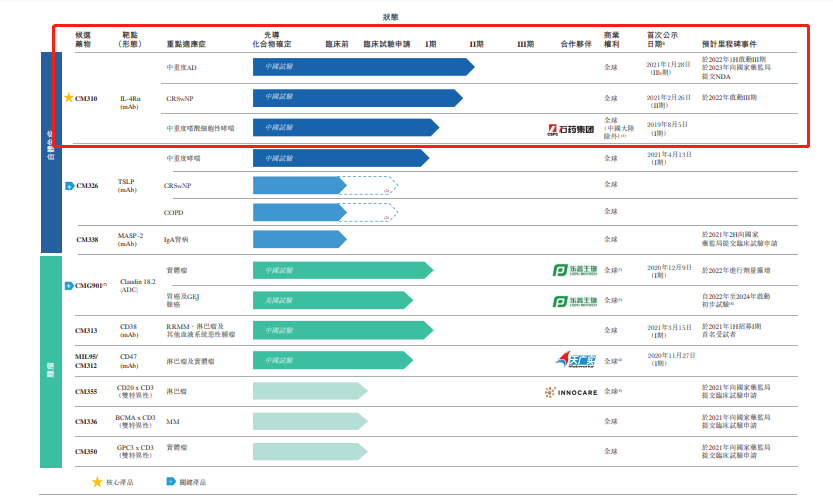
招股书显示,康诺亚的核心产品CM310可用于治疗自免疾病,另外2款重磅产品CM326、CMG901可分别用于自免及肿瘤疾病的治疗。
截图自招股书
CM310是一种针对IL-4Rα的高效、人源化拮抗性抗体。其中,IL-4Rα属于2型炎症通路中I型受体和II型受体的关键组成部分,因此通过作用IL-4Rα可同时阻断白介素4(IL-4)及白介素13 (IL-13)两个2型免疫反应的强效调节因子信号传导,有望有效治疗各种成人、青少年及儿童Ⅱ型过敏性疾病(重度特应性皮炎、中重度嗜酸性哮喘、慢性鼻窦炎拌鼻息肉)及潜在慢性阻塞性肺病。
值得一提的是,CM310是首个国产且获批临床的IL-4Rα抗体,其治疗特应性皮炎的适应症已进入临床II期,预计2023年将向NMPA递交NDA申请;治疗慢性鼻窦炎的适应症预计于2022年启动III期临床。
CM326为针对胸腺基质淋巴细胞生成素(TSLP)的高效、人源化单克隆抗体,是中国首个、全球第三个获批临床的国产TSLP靶向抗体。其中,TSLP是一种重要的、介导多种炎症途径的上游细胞因子,通过靶向TSLP、CM326抑制导致过敏及其他疾病的异常炎症反应。CM326可用于治疗各种过敏性疾病,包括中重度哮喘(嗜酸性粒细胞依赖性和非依赖性)及慢性鼻窦炎伴鼻息肉,且有望治疗慢性阻塞性肺疾病,目前处于临床I期。
CMG901为靶向Claudin18.2的抗体偶联药物,含Claudin 18.2特异性抗体、可裂解连接符及毒性载荷单甲基澳瑞他汀E(MMAE),是首个在中国及美国取得临床试验申请的Claudin 18.2抗体偶联药物,可用于治疗胃癌、胰腺癌及其他Claudin 18.2高表达实体瘤。目前尚无靶向Claudin 18.2的药物获批上市。其中,康诺亚的CMG901与石药集团的SYSA1801为国内申报的Claudin 18.2 ADC药物。
此外,康诺亚管线中还包含MASP-2抗体、CD38抗体、CD47抗体、CD20xCD3双抗、BCMAxCD3双抗及GPC3xCD3双抗在内的热门靶点药物,目前全球尚未有MASP-2抗体获批上市。
整体来看,康诺亚采用自免+肿瘤双驱动模式,一方面通过IL-4Rα抗体CM310、TSLP单抗CM326、MASP-2单抗CM338差异化布局自身免疫领域以占领接下来超160亿美元的国内市场份额。另一方面通过单抗、ADC、双抗多方面布局肿瘤领域,且靶向Claudin18.2、CD47、CD38等热门靶点,市场增长空间较大。
此外,CM310正在同时进行有关中重度特应性皮炎、慢性鼻窦炎伴鼻息肉、中重度哮喘3项适应症的临床试验。
据Frost & Sullivan数据,与CM310目前适应症有关的药品在2019年的市场规模总值高达45亿美元(约300亿人民币)。
此外,自度普利尤单抗自上市以来,IL-4Rα的全球市场已从2017年的2亿美元以153.9%的年复合增长率大幅增至2020年的40亿美元,随着适应症的不断扩展及IL-4Rα靶向药物渗透率增加,预计到2030年,IL-4Rα的全球市场可达287亿美元。
据相关统计,全球共有7种IL-4Rα药物处于临床及以上阶段,但绝大多数仍处在I、II期临床阶段,而在国内康诺亚、康奈德的项目均处于临床II期,进度最快。不过康诺亚为了更好地实现CM310在中重度哮喘和慢性阻塞性肺病等呼吸系统疾病领域的商业化布局,已和石药集团达成独家授权合作,因此CM310也有望成为首款国产IL-4R产品。
祝贺康诺亚成功上市,有关康诺亚的后续进展贝壳社也将保持关注。


文章评论(0)