从追捧到相继退出,SHP2抑制剂还值得被期待吗?
但近年来,SHP2靶向药研发逐渐取得突破,研究人员开发了对SHP2具有显著抑制作用的变构抑制剂,并且在实体肿瘤上进行的临床试验取得显著进展。诺华、艾伯维、辉瑞、加科思等国内外企业开始聚焦SHP2靶点,投身SHP2抑制剂的“拓荒”队伍。但是SHP2靶点难以成药的特点,使得赛道上的选手走得比较波折, 有人坚守研发,有人中途退场,在争议声中,SHP2负重前行,逐渐成为当下热度持续攀升前沿抗癌靶点之一。

图源:加科思官网
我们知道,加科思在SHP2抑制剂的开发处于国际领先地位,因此其旗下两款SHP2 抑制剂JAB-3068 和 JAB-3312备受瞩目,并在2020年得到艾伯维的青睐。
2020年6月,艾伯维以4500万美元首付款,8.1亿美元里程碑付款和一定比例销售分成,从加科思引进了两款SHP2抑制剂的全球权益。2022年,加科思又收到2000万美元里程碑付款。
根据协议,双方将共同开发加科思自主研发的这两款小分子抗肿瘤药 SHP2 抑制剂,产品上市后,加科思拥有大中华区的全部商业化权益,而艾伯维将负责海外市场销售,加科思将收到一定比例的销售提成。
然而时隔3年,在加科思加码推进SHP2抑制剂研发的档口,艾伯维宣布与加科思分手,退出SHP2抑制剂赛道。
其实,这不是SHP2抑制剂研发史上的第一个“分手”事件。在2022年的12月,赛诺菲方面发出通知,终止与Revolution Medicines从2018年开始价值5亿美元的SHP2抑制剂RMC-4630的开发和商业化合作。协议终止后,Revolution Medicines将重新获得赛诺菲根据协议获得的所有全球权利,包括关于研发的决策权,以及RMC-4630的所有商业收益权。
曾经艾伯维与加科思,赛诺菲与Revolution Medicines在SHP2抑制剂赛道的牵手,一度让SHP2大受追捧,从不温不火的小靶点加速逆袭成明星靶点。如今这两笔关于SHP2抑制剂的资本合作,半路就“无疾而终”,不免让人感慨SHP2抑制剂真的没有未来了吗?
SHP2作为一种非受体蛋白酪氨酸磷酸酶,在受生长因子、细胞因子和整合素受体调节的细胞信号转导下游发挥重要作用,并参与包括细胞存活、增殖和迁移在内的细胞过程。
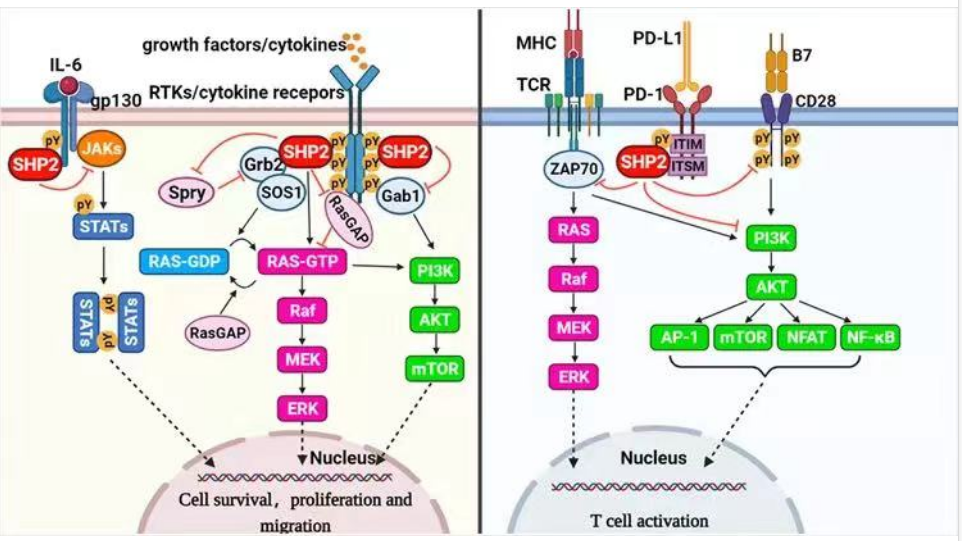
SHP2介导的信号通路
图源:加科思招股书
越来越多的证据表明,SHP2参与了癌细胞中的许多信号级联,包括RAS-MAPK、PI3K-AKT和JAK-STAT通路。对于PD1-PDL1通路的影响也在研究中其次,Th1免疫能力的恢复和T细胞的激活也依赖于SHP2的抑制,Th1免疫能力的恢复和T细胞的激活能够激活肿瘤微环境内的免疫反应。通过对SHP2的药理抑制可以增强CD8+ 细胞毒性T细胞介导的抗肿瘤免疫来降低肿瘤负担。
基于SHP2靶点在激活RAS蛋白和执行PD1信号通路上的功能,SHP2抑制剂和PD1单抗、KRAS抑制剂的联用潜力巨大,PTP结合位点的传统抑制剂,如PHPS1、GS-493和NSC-87877普遍存在细胞渗透性低和生物利用度差的问题。
例如诺华的TNO-155,是全球首款进入临床阶段的SHP2抑制剂。在2021年ASCO年会上,诺华公布报告了TNO155在成年晚期实体瘤患者中的I期临床试验初步结果。结果显示,截至2021年2月8日,在入组的125名患者中,客观缓解率为0%,更是有94%的患者因为疾病进展、不良反应、死亡而停止了治疗,因此证明SHP2抑制剂的单药效果不佳。
所以说当前SHP2抑制剂的研发主要用在联合疗法上,也就是说一家企业若想推动其SHP2抑制剂快速上市,基本要联合用药才有出路,而PD-1和KRAS抑制剂是最佳搭档选择。
从联药角度来看,艾伯维要想从中获益,需要在自身管线中投入PD-1和KRAS抑制剂进行联药研究,而这刚好是艾伯维的管线弱点,因为其管线内既没有PD-1也没有KRAS。
而赛诺菲的RMC-4630由于其在RAS-MAPK通路上的作用,可以与KRAS G12C抑制剂Sotorasib、Adagrasib联用,虽说Sotorasib与RMC-4630的联用展现出了较好的初步效果,但是但局限在肿瘤领域,而赛诺菲在肿瘤赛道并没有优势,RMC-4630联合用药需要花费大量财力物力,赛诺菲权衡利弊之后退出SHP2赛道。
PD-1抗体药物上市后,仍有大部分肿瘤患者对其响应不佳或很快产生耐药,部分原因在于患者的肿瘤组织中无明显的T细胞浸润或存在大量的免疫抑制性巨噬细胞,是所谓的“冷肿瘤”。通过同时作用于T细胞和巨噬细胞,最大化激活抗肿瘤免疫反应,SHP2抑制剂可能将“冷肿瘤”变为“热肿瘤”,进一步提高PD-1疗效,并克服PD-1耐药。
SHP2靶点是介导多条RTK信号传导到RAS的关键磷酸酶,SHP2抑制剂可以阻断所有应用KRAS G12C抑制剂产生耐药模型中的RAS通路的负反馈激活,SHP2抑制剂(JAB-3312)联合KRAS G12C抑制剂(JAB-21822)从机制上可能能够增强对RAS通路的持续抑制性,增强体内外抗肿瘤活性,并且也有可能解决患者对KRAS抑制剂单药耐药的问题,提高疗效和解决耐药的有效策略。
据弗若斯特沙利文分析,2018年全球PD-(L)1抑制剂的市场规模为163亿美元,到2023年预计将达639 亿美元。而在中国,预计2023年PD-(L)1抑制剂的市场规模将达664亿元人民币,2030年则将增长至988亿元人民币。
另外根据观研报告网数据显示,约有40%-50%的结直肠癌患者、30%的非小细胞肺癌患者及80%-90%的胰腺癌患者存在KRAS突变阳性,KRAS靶向药物临床需求巨大且尚未满足。2016-2020年,全球主要KRAS突变阳性癌症的发病人数从180万人上升至200.9万人,预计2023年将达到216.5万人,KRAS抑制剂极具市场前景,当前的研发已经渐入佳境。
由此可见,在PD-(L)1及KRAS抑制剂广阔的市场前景下,SHP2抑制剂联合PD-1及KRAS抑制剂有望克服耐药性问题,极具潜力,临床开发值得期待。
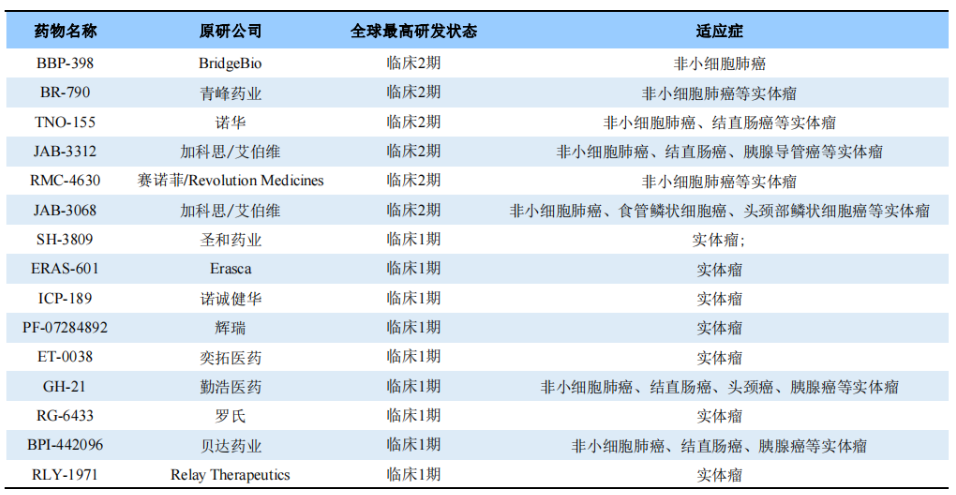
全球已进入临床试验阶段的SHP2抑制剂
图源:药渡数据
纵观全球研发SHP2抑制剂的企业,无论是Revolution、罗氏、诺华,还是本土企业加科思等,都在积极开展SHP2抑制剂与PD-(L)1抗体及KRAS抑制剂的联合用药试验。比如,加科思的JAB-3312/JAB-21822、Revolution Medicines的RMC-4630联合KRAS G12C,罗氏的GDC-1971联用PD-1抗体Atezolizumab,诺华TNO155联用PD-1抗体Spartalizumab等。
国际赛道上,诺华跑得最快。诺华公司于2016年《nature》发布的全球首款SHP2变构抑制剂,SHP099可同时结合N-SH2、C-SH2和PTP结构域界面并与这三个结构域中的关键氨基酸残基产生氢键相互作用。
之后基于KRAS-G12C抑制剂与SHP099的联用也会显著提高某些肿瘤(携带KRASG12C突变)的抗肿瘤免疫效应,诺华在此基础上对SHP099做了优化,推出了TNO155,成为首款进入临床开发的SHP2变构抑制剂。
赛诺菲退出之后,Revolution表示,会继续单方面推进RMC-4630的研发,以评估RMC-4630与Sotolasib联合治疗携带KRAS G12C突变的NSCLC患者,目前RMC-4630进入II阶段临床试验。
Bridge Bio的BBP-398也是一款进入II期临床实验的SHP2抑制剂。2022年5月,BridgeBio Pharma与BMS的一笔关于BBP-398的高达9亿美元的交易一时间让SHP2靶点又热度高升。目前Bridge Bio对BBP-398单药和联合治疗实验已进入II期临床试验。
此前,BridgeBio已经与联拓生物达成合作,由联拓生物在中国及其它主要亚洲市场进行BBP-398的临床开发和商业化。目前,联拓生物正在中国进行该药的Ib期临床组合疗法的研究。
回归国内赛道,加科思一马当先。加科思作为继诺华之后,全球第二家,国内第一家进行SHP2抑制剂临床研究的企业,已手握两款SHP2抑制剂(JAB-3068 和 JAB-3312),已然跑到全球SHP2抑制剂研发的最前端。
值得注意的是加科思的JAN-3312已经完成了升级,属于第二代SHP2抑制剂,且是目前唯一的一款第二代SHP2抑制剂。与第一代SHP2抑制剂相比,SHP2抑制剂具备用药剂量更小、可以采用非间歇性给药模式、提升药效和降低毒性等优势,具备更强大的抗肿瘤活性(第二代的活性比第一代强20倍)及更高的成药性的可能。
2020年9月,FDA授予了JAB-3312治疗食管癌的孤儿药资格认定,可用于支持该药在食管癌适应症上的全球开发。加斯科目前开展JAB-3312联合Glecirasib(加科思自己的KRAS G12C抑制剂)的临床实验,相关数据预计将于今年下半年发布。
另外加科思JAB-3068是全球第二个进入临床的SHP2抑制剂,JAB-3068单独口服给药能够促进CD8+ T细胞杀伤肿瘤的功能,也可以与PD1/PD-L1抗体联合应用,目前,JAB-3068用于PD-1/PD-L1抗体无应答的肿瘤治疗,临床进入II期。
另外,国内布局SHP2抑制剂的企业还有圣和药业、诺诚健华、勤浩医药、贝达药业等。
创新药的研发,坚守到底的不一定笑到最后,中途退场的也不一定满盘皆输,这就是探索未知结果的魅力所在。
虽然屡屡被放弃,但是SHP2抑制剂研发依旧未来可期。
参考资料:
1、《加科思JAB-3312 获得FDA孤儿药资格认定》生物制药之家,2020年10月20日
2、《SHP2 抑制剂有何魔力?BMS 和 BridgeBio 达成 9 亿美元独家许可协议,共同开发和商业化 BBP-398》凯来英药闻,2023年5月13日
3、《SHP2抑制剂被艾伯维“退货”,加科思-B(01167)股价遭重未来何寻?》智通财经,2023年7月5日
4、《继赛诺菲后!艾伯维退回加科思SHP2抑制剂全球权利》Medaverse,2023年7月4日


文章评论(0)