Ascendis将迎来80亿美元机会之窗
Ascendis呼唤甲状旁腺功能减退的新激素替代品。
该丹麦生物制药公司现在面临着迅速采取行动以利用这一偶然的机会之窗,证明其Transcon PTH可能成为成人甲状旁腺功能减退症的一种新疗法。
事情是这样的。去年9月,武田宣布在美国召回所有剂量规格的NATPARA(甲状旁腺激素)注射液(25mcg、50mcg、75mcg、100mcg),从美国市场撤出。Ascendis希望监管机构的能够批准它立即开始美国的关键试验,这将有助于其赢得80亿美元的市场。
值得一提的是,早在2018年6月,美国FDA已经授予Ascendis公司长效甲状旁腺激素前体药物TransCon PTH孤儿药地位。
TransCon PTH是一种长效的甲状旁腺激素(PTH)前药(prodrug),采用Ascendis公司创新性的TransCon技术开发。TransCon PTH旨在恢复PTH至生理水平,使血液和尿液钙水平、血清磷酸盐水平、骨转换正常化。
Transcon PTH背后的逻辑是PTH长效前药的巧妙递送,甲状旁腺功能减退症患者生产的PTH量不足。目的是克服Natpara的问题-可变的PTH水平; Natpara也与钙失衡有关,并带有黑框警告,提示骨肉瘤。
Ascendis早些时候报告了Transcon PTH II期试验的受控部分的积极数据,并且从长期结果来看,该公司已着手修改其美国IND,以允许III期尽快开始。
最新结果与中期研究的开放式标签延长六个月有关。该扩展程序已经开放给各个剂量和控制部门的所有59位参与者,其中58位入选。 被拒绝的受试者可能是“出于与Transcon PTH的安全性或有效性无关的原因”。
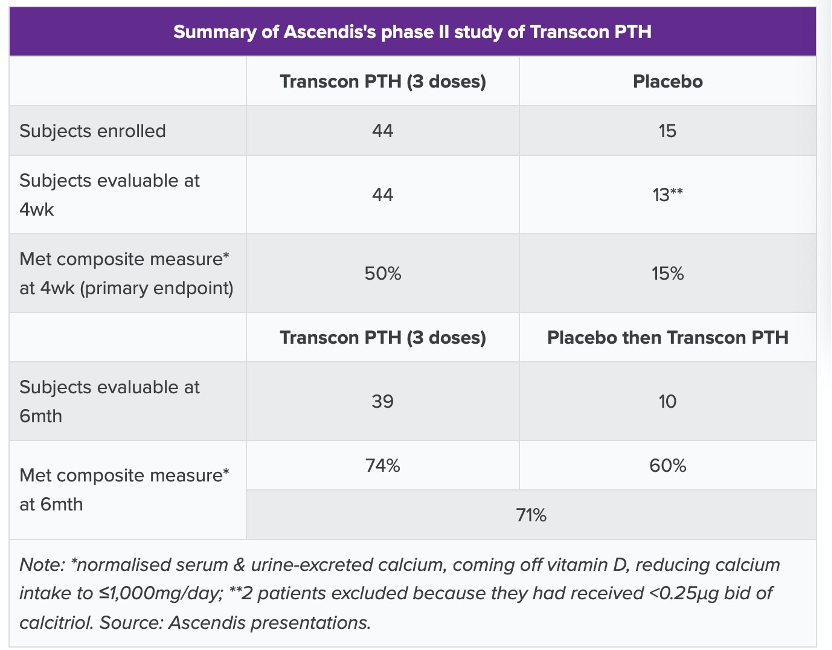
在为期4周的治疗阶段后,三种剂量共44位受试者中有50%达到了主要终点,结果显示血清和尿液分泌的钙正常化,脱离了维生素D,并将钙摄入量减少至1,000mg / day或更低。 相比之下,13位安慰剂接受者中,有15%达到了这一终点。
随着试验的推进,数据只会越来越好——如果忽略掉几名失踪的患者。所有四个队列中的49名受试者在六个月时都有可用数据,其中71%的患者在此后的时间点达到了综合主要疗效指标。
Ascendis说,三名受试者的尿液样本未正确制备,实验室未收到另外两份。由于缺少169-210天的尿液采样窗口,其余的四个遗漏的受试者被排除在外。Ascendis解释说,所有这四个人实际上都不含维生素D,并且所含钙补充剂≤500mg,其中三个人的血清和尿钙水平正常。
开放标签扩展数据支持计划的关键研究,该研究将有六个月的主要终点。该综合措施与第二阶段略有不同,第二阶段仅包括血清钙正常化,维生素D独立性和≤600mg钙补充。
尿钙正常化将是第三阶段的次要措施。该计划是将57名受试者接受中期中等剂量的Transcon PTH(18µg /天),并将19名受试者随机分配给安慰剂。
在9月29日的分析师电话会议上,Ascendis表示,根据各种假设,在49位可评估的II期受试者中,有45位将达到III期终点。计划中的研究“具有极大的成功动力”。
甲状旁腺功能减退症是一种罕见的内分泌疾病,其特征是PTH水平不足导致血液中钙含量低以及磷酸盐水平升高。
据估计,甲状旁腺功能减退症影响美国约80000例患者,大多数患者在甲状腺手术期间损伤或意外切除甲状旁腺后发生病情。在短期内,症状包括:虚弱,肌肉痉挛,异常感觉,如刺痛、灼烧和麻木,记忆力丧失,判断失误和头痛。患者常常体验到生活质量的下降。长期而言,这种复杂的紊乱会增加主要并发症的风险,如骨骼外钙沉积,发生在脑内、眼晶状体和肾脏,其中钙在肾脏内沉积可能导致肾功能受损。
甲状旁腺功能减退症的常规疗法维生素D和钙补充剂并不能完全控制疾病,并可能因钙尿增加引起渐进性肾脏钙化和肾结石,导致肾脏疾病。。结果,与健康人相比,甲状旁腺功能减退症患者发生肾脏疾病的风险高出四倍。


文章评论(0)