后PD-1时代,双抗热点迸发,500亿市场即将开启
作者丨北北
近年来,肿瘤治疗已经进入免疫治疗时代,尤以抗PD-1单抗为代表的免疫检查点抑制剂进展最快,也实现了多个实体瘤领域的突破。但免疫检查点抑制剂单药应用,由于患者响应人群数量较低,耐药率较高等弊端,限制了其在临床中的推广应用,如何有效突破免疫单药的困局,当前也有几条可行的途径:
PD-1/CTLA-4双抗
PD-1和CTLA-4联合阻断,最经典的双免疫组合方案就是纳武利尤单抗联合伊匹木单抗的“O+Y”组合,已经被应用于包括肝癌、黑色素瘤等多个癌种的适应症。但由于CTLA-4单抗的剂量依赖性毒副作用,使得联合疗法中,CTLA-4单抗治疗剂量受到限制。因此,迫切需要结合找到安全有效的方式,靶向PD-1和CTLA-4的双特异性单克隆抗体就是一种好的设计方式。
布局PD-1/CTLA-4双抗的企业众多,进展最快的是国内的康方生物自研产品AK104。
2021年9月,CDE已经受理卡度尼利单抗(AK104)治疗复发/转移宫颈癌的新药上市申请,并给予优先审评资格。
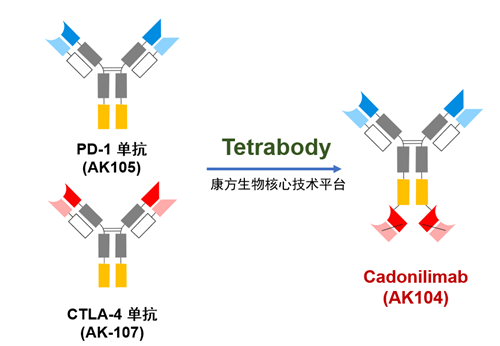
图1. Tetrabody技术平台
该双抗是基于康方生物的Tetrabody核心技术平台,将康方自主研发的、已经获批上市的抗PD-1单抗(派安普利单抗)的全部结构与授让给默沙东的抗CTLA-4单抗(AK107、MK1308)的scFv片段结合,最终形成了可靶向PD-1和CTLA-4靶点的人源化四聚体双特异性抗体—AK104。
AK104作用机制如下:
此外,肿瘤微环境中活化的巨噬细胞通过分泌促炎细胞因子,如IL-6和IL-8,在介导免疫抑制中发挥关键作用。Fc段改造,旨在消除与FcγRs和C1q的结合,从而最大限度地减少淋巴细胞损失和巨噬细胞释放抗体依赖性细胞因子,从而有效减少irAE和免疫治疗中的不良预后。
MEDI5752,是一款经过工程化改造,降低了FC效应器功能的单价双特异性人IgG1单克隆抗体。
MEDI5752采用的是DuetMab技术,即二硫键移位避免轻链错配。由于单价形式,MEDI5752对于PD-1和CTLA-4的阻断效应是有所减弱的。
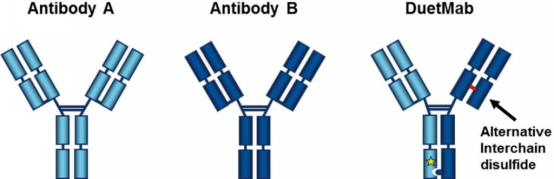
图2. DuetMab技术
虽然价态和结构与AK104有所不同,但在《Cancer Discovery》上发表的MEDI5752基础研究试验结果,为PD-1/CTLA-4双抗在临床上表现出的更好疗效、更低毒性的效果给出了具体机制。
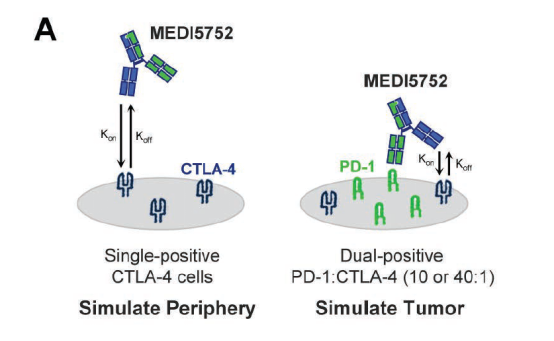
图3. MEDI5752的靶点结合
MEDI5752对活化的PD-1+T细胞的CTLA-4优先抑制。上图所示,与PD-1-T细胞相比,MEDI5752优先饱和PD-1+T细胞的CTLA-4。
此外,值得一提的是,MEDI5752也会导致PD-1的内吞和降解,并且可以优先在肿瘤微环境(TME)中积聚,在阻断PD-1通路的同时,在TME中提供更强的CTLA-4抑制作用。与PD-1和CTLA-4的单抗组合相比,表现出增强的抗肿瘤活性。
2022年的AACR大会摘要显示,在1期临床试验中,这一疗法在治疗不适合标准治疗的晚期实体瘤患者时表现出可喜的抗癌活性。
综合不同剂量,客观缓解率为19.8%,中位缓解持续时间为17.5个月。生物标志物分析显示MEDI5752强力阻断PD-1和CTLA-4信号传导,并且显示出扩展已有或新T细胞克隆的潜力。

图4. 在研PD-1/CTLA-4双抗
除了PD-1/CTLA-4双抗有不少企业布局以外,PD-L1/CTLA-4双抗也是当下的研究热点,进度最快的是康宁杰瑞的KN-046。

图5. KN046晶体结构
KN046是康宁杰瑞自主研发的PD-L1/CTLA-4双特异性抗体,其创新设计包括:采用机制不同的CTLA-4与PD-L1单域抗体融合组成,可靶向富集于PD-L1高表达的肿瘤微环境及清除抑制肿瘤免疫的Treg。多项实体瘤项目已经推进到III期阶段。
PD-1/LAG 3双抗
LAG-3(淋巴细胞活化基因3),是抑制型免疫检查点,主要在T细胞上表达,其作用机制如下:
主要与MHC II结合,负向调节T细胞增殖和活化;
可与Galectin-3、LSECtin结合,影响 T 细胞的功能;
与纤维蛋白原样蛋白1(FGL1)结合,促进肿瘤免疫逃逸。
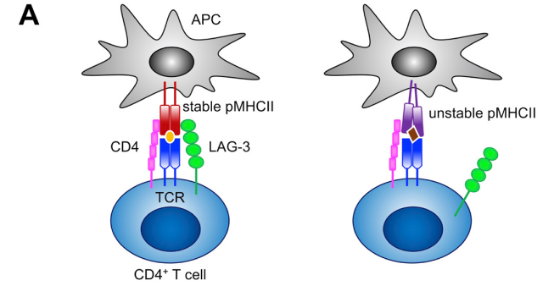
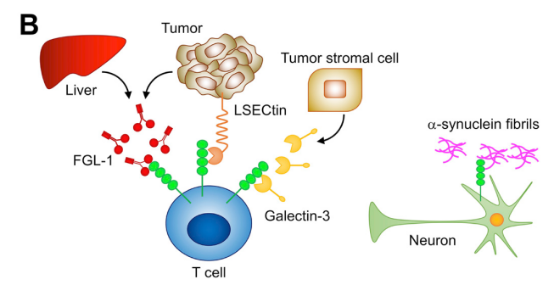
图5. LAG-3靶点的作用机制
2022年3月18日,FDA正式批准施贵宝公司的抗LAG-3单抗(Relatlimab)联合自家的抗PD-1单抗(Nivolumab)的联合方案用于转移性黑色素瘤的治疗。Relatlimab也由此成为施贵宝公司继Nivolumab、Ipilimumab之后第三款获批上市的免疫检查点抑制剂。
对LAG-3单抗来说,单药治疗效果有限,联合抗PD-1单抗拓展适应症,成为研发的主流趋势。而随着双特异性抗体的火热,也有企业开始加速布局PD-1/LAG-3双抗。
例如,罗氏开发的PD-1/LAG-3双抗(RO7247669注射液)在全球范围内积极开展1/2期临床试验,涵盖的拟开发适应症有:晚期肝细胞癌、转移性黑色素瘤、非小细胞肺癌、食管鳞状细胞癌、转移性食管癌等。
国内布局的企业有:岸迈生物(EMB-02,PD-1/LAG-3双抗)、康方生物(AK-129,PD-1/LAG-3双抗)、再鼎医药(MacroGenics合作的MGD013,PD-1/LAG-3双抗)。
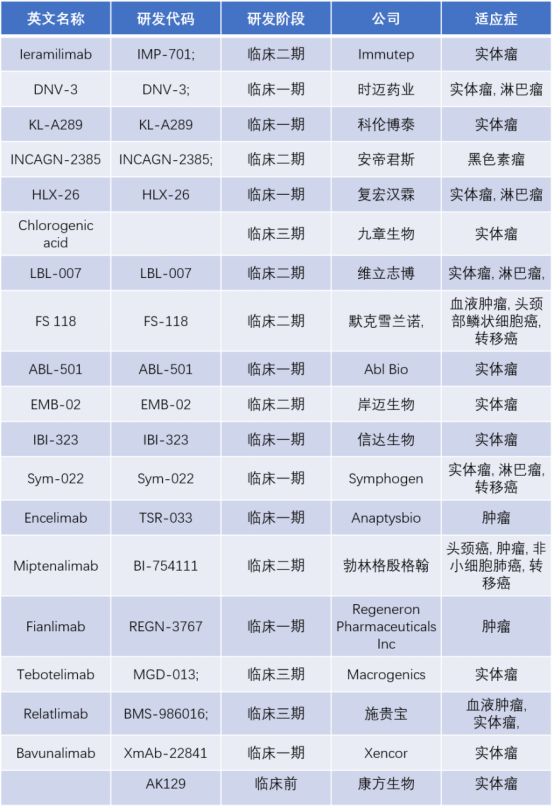
图6. PD-1/LAG3双抗在研产品
PD-L1/TGF-β 双抗
近年来,靶向肿瘤微环境相关因子的双抗也逐渐增多,靶点包括VEGF、VEGFR2、TGF-β等,最具代表性的就是PD-L1/TGF-β双抗,但多为失败的例子。
2021年8月23日,德国默克宣布终止 M7824(PD-L1/TGFβ双抗)联合化疗一线治疗胆管癌的二期临床,因为不太可能达到OS终点,研究未发现新的安全信号。此次终止也成为M7824失败的第三项临床研究。过往还有两项试验(肺癌、胆管癌二线)未能达到预期。
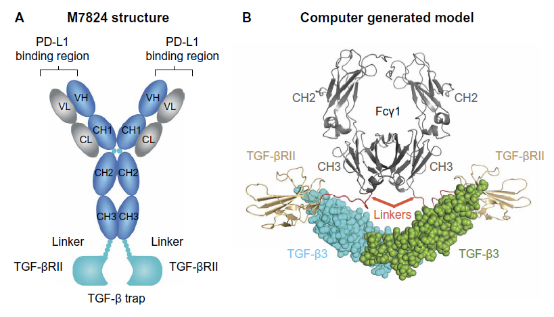
图7. M7824的结构和模型
理论上,TGF-β是一种在肿瘤发生晚期表达大幅升高的肿瘤促进因子,通过诱导免疫逃逸、促进血管形成、诱导上皮间质转化,促进肿瘤细胞的生长、浸润与转移。PD-L1也在肿瘤细胞上高度表达,阻断PD-L1和TGF-β两个靶点,应该能够带来明显的抗肿瘤活性。但M7824的接连失败,为PD-L1/TGFβ双抗的研发未来蒙上了一层阴影。
PD-L1/4-1BB 双抗
PD-L1/4-1BB双抗,进展最快的是BioNTech公司的GEN1046(PD-L1×4-1BB)双抗,近期,也发表了GEN1046人体临床前特征和首次人体研究结果。
GEN1046是一个全长IgG1亚型、 PD-L1×4-1BB双抗,使用DuoBody®技术平台,通过单克隆全人源PD-L1和人源化4-1BB抗体的Fab臂交换产生,基于双特异性模式的体外生物活性选择母代PD-L1和4-1BB抗体。母代抗体包含CH3结构域的对应突变F405L/K409R(促使Fab臂的异源二聚化,生成双特异性分子)和Fc沉默突变 L234F/L235E/D265A(阻止结合FcγR和C1q,去除ADCC、ADCP和CDC效应)。
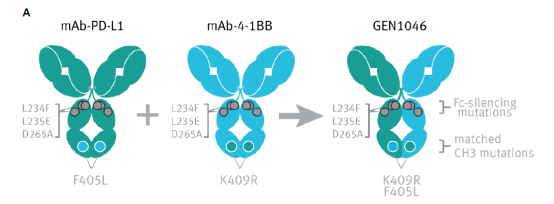
图8. GEN1046的结构
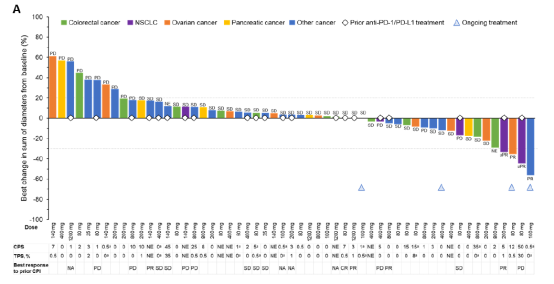
图9. GEN1046在晚期实体瘤患者中的抗肿瘤疗效
初期表现出不错的临床治疗效果和安全性,期待更大样本量的研究数据积累。
国内布局此靶点的双抗及多抗的企业也较多,都处于临床早期阶段,汇总如下:
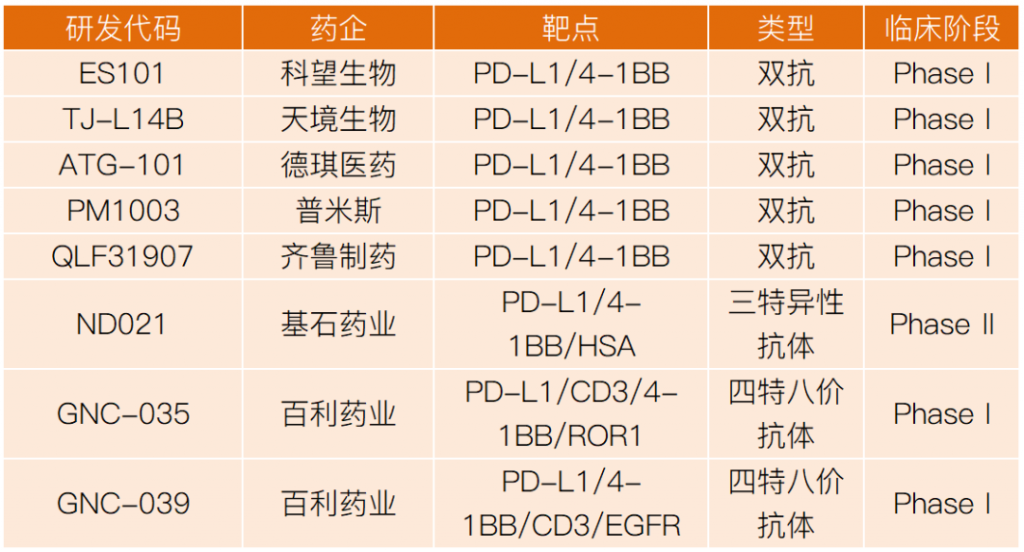
图10. 国内4-1BB的双抗及多抗在研产品
双抗联合双抗
基于双抗能够耐受的安全性和抗肿瘤活性,以双抗为基础的多靶点联合方案,也有不少企业开始尝试。
2022年1月5日,康方生物宣布,其自主研发的全球首创新型肿瘤免疫治疗新药AK104 (PD-1/CTLA-4双抗、卡度尼利单抗)联合AK112(PD-1/VEGF双抗)Ib/II期临床试验申请获CDE批准,联合或不联合化疗治疗晚期非小细胞肺癌(NSCLC)。
康宁杰瑞也正在尝试KN026(HER-2/HER2双抗)联合KN046(PD-L1/CTLA-4双抗)治疗HER-2阳性实体瘤的疗效和安全性。
2022年AACR大会上也公布了初期结果。截至2021年8月10日,共入组24例接受过≥1L系统治疗、HER2阳性非乳腺癌和胃癌、局部晚期不可切除或转移性实体瘤患者,20例患者接受至少一次肿瘤评估:客观缓解率(ORR)为55.0%,疾病控制率 (DCR) 为85.0%,6个月的PFS率为84.1%;其中11名可评估的结直肠癌患者ORR和DCR分别为45.5%和90.9%。
总 结
目前双抗已成为继PD-1、CAR-T、抗体偶联药物等热门赛道之后的又一大热门风口。随着全新双抗进入市场,同时已上市双抗获批更多适应证,双抗的全球市场规模在2025年将超过500亿元。为此全球药企巨头相继加入研发大军,开启竞赛模式。
鉴于当下双抗药物研发逐步火热,为了防止陷入无效竞争,浪费医疗资源,2022年4月11日,为进一步规范双特异性抗体类抗肿瘤药物的临床研发,CDE发布《双特异性抗体类抗肿瘤药物临床研发技术指导原则(征求意见稿)》,面向业界征求意见。对于双抗一众从业者提出了更高的要求,如何有效弥补免疫单抗药物尚不能满足的临床需求,靶点选择是否合理,都是亟待解决的问题。
参考文献


文章评论(0)