两款新药拟获突破性疗法认定,来自信达、亚盛
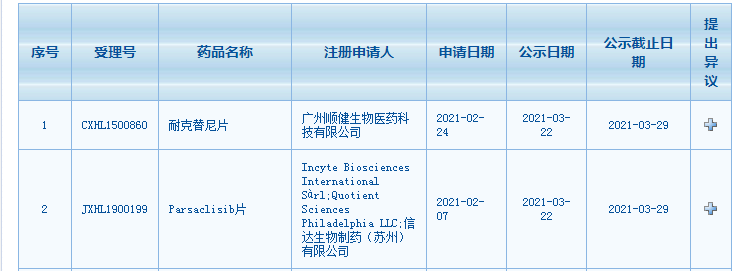
3月22日,国家药品监督管理局药品审评中心(CDE)官网最新公示,信达生物制药(苏州)有限公司(信达)的Parsaclisib片以及广州顺健生物医药科技有限公司(亚盛医药全资子公司)的耐克替尼片已纳入拟突破性治疗品种。
截图自CDE
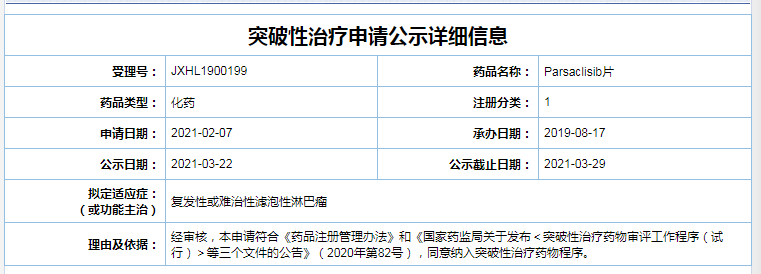
Parsaclisib片
适应症:拟用于复发性或难治性滤泡性淋巴瘤
公司:信达生物
截图自CDE
Parsaclisib是一种强效、高选择性、新一代磷脂酰肌醇3-激酶δ(PI3Kδ)口服抑制剂,对于抑制PI3Kδ在恶性B细胞淋巴瘤的生长、存活中起关键作用。2018年12月,信达与Incyte达成战略合作,由此获得Parsaclisib在中国大陆及港澳台的开发和商业化权利。
Incyte正在评估Parsaclisib作为单一疗法在数项II期试验中对非霍奇金淋巴瘤(滤泡性淋巴瘤、边缘区淋巴瘤和套细胞淋巴瘤)和自身免疫性溶血性贫血的治疗效果。2019年12月,Parsaclisib在国内获批临床,用于复发/难治滤泡性淋巴瘤和边缘区淋巴瘤。此外,Incyte也正在进行Parsaclisib联合ruxolitinib治疗骨髓纤维化患者的注册临床试验。Incyte还计划开展一项Parsaclisib联合tafasitamab治疗弥漫性B细胞淋巴瘤的评估试验。
2020年12月,信达在ASH2020上公布Parsaclisib用于治疗复发或难治性滤泡性淋巴瘤(CITADEL-203)和边缘区淋巴瘤(CITADEL-204)的II期研究结果。数据显示,Parsaclisib用于治疗复发或难治性滤泡性淋巴瘤的客观缓解率(ORR)为75%,中位无进展生存期(mPFS)为15.8。Parsaclisib用于治疗复发或难治性边缘区淋巴瘤的ORR为56.9%,mPFS为19.4。在所有研究中,Parsaclisib普遍耐受性良好,安全性可控。
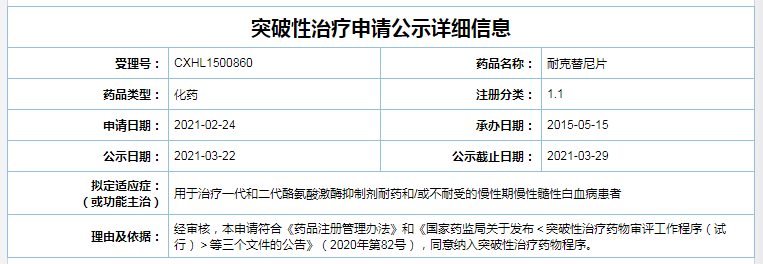
耐克替尼片
适应症:拟用于治疗一代和二代酪氨酸激酶抑制剂耐药和/或不耐受的慢性期慢性髓性白血病患者
公司:亚盛医药
截图自CDE
耐克替尼(HQP1351)是第三代BCR-ABL抑制剂,也是国内首个第三代BCR-ABL靶向耐药慢性髓性白血病(CML)治疗药物。对BCR-ABL以及包括T315I突变在内的多种BCR-ABL突变体有突出疗效。2020年5月,HQP1351先后获得FDA授予的孤儿药资格和快速审批资格。2020年9月,HQP1351正式被NMPA纳入优先审评,用于治疗酪氨酸激酶抑制剂(TKI)耐药后并伴有T315I 突变的CML慢性期或加速期的成年患者。
2020年11月,亚盛医药的原创1类新药BCR-ABL抑制剂HQP1351的两项关键性注册II期临床研究结果入选第62届美国血液学会(ASH)年会的口头报告。这两项研究数据显示,HQP1351在伴有T315I突变的TKI耐药的慢性期及加速期的患者中均具有良好的疗效及耐受性。
CML是一种与白细胞有关的恶性肿瘤。目前主要以靶向BCR-ABL的TKI药物治疗为主,然而随着第一代BCR-ABL抑制剂伊马替尼(格列卫)及后续推出的几种二代药物成功上市,耐药性便成为治疗CML的主要挑战。而BCR-ABL激酶区突变是获得性耐药的重要机制之一,其中T315I突变是常见的耐药突变类型之一,伴有T315I突变的CML患者对目前所有一代、二代BCR-ABL抑制剂均耐药,因此临床上急需有效的第三代治疗药物。


文章评论(0)