首日高开超91%!映恩生物正式港股上市
今日,映恩生物正式港交所上市,股票代码为09606.HK。映恩生物此次IPO的全球发售股份数量为1507.16万股。其中,香港公开发售占总发行量的10%,国际发售占90%。此外,本次发行还设有15%的超额配售权(绿鞋期权)。共引入15位基石投资者,认购金额6500万美元。
映恩生物在招股书中表示,IPO募集所得资金净额将主要用于核心产品的研究、开发和商业化,特别是DB-1303/BNT323和DB-1311/BNT324。资金还将用于关键产品的研发,为ADC技术平台的持续开发提供资金,推进其他管线资产以及探索和开发新药物资产,并用作运营资金及其他一般公司用途。
日前,映恩生物公布配发结果,香港公开发售股份数目(经重新分配后调整)为753.58万股,国际发售股份数目(经计及发售量调整权获悉数行使及经重新分配后调整)为979.65万股。最终发售价为94.6港元/股,全球发售净筹约15.13亿港元,其中,香港公开发售获115.14倍认购,国际配售获13.52倍认购。映恩生物IPO前最后一轮融资后估值为2.7亿美元,按发售价94.6港元计算,估值11亿美元,估值step-up达到307%,成为历史上估值step-up最大的18A项目。
映恩生物已与海内外多个跨国药企达成多项授权合作,交易总金额超60亿美元,如BioNTech、百济神州、GSK、Avenzo等,这突显了其早期资产和技术平台的价值。
作为一家临床阶段的生物制药公司,映恩生物目前处于亏损阶段,这主要是由于缺乏商业化的产品以及持续大量投入研发活动。财报显示,2022年至2024年,公司累计亏损约17.95亿元。
在IPO之前,映恩生物成功完成了四轮融资,总额达1.38亿美元。公司的投后估值从最初的1450万美元增长到IPO前的2.7亿美元(约合19.72亿元)。
此外,来自对外授权的大额收入为映恩生物的运营和研发活动提供了重要的非稀释性资金来源。
映恩生物拥有由12款内部自主研发的ADC候选药物组成的强大管线。其中包括7款处于临床阶段的ADC,2款新一代双特异性ADC和1款治疗自身免疫性疾病的ADC预计将于2025年至2026年进入临床阶段。其两个核心产品是DB-1303/BNT323(靶向HER2的ADC候选药物,适用于包括子宫内膜癌和乳腺癌在内的多种癌症)和DB-1311/BNT324(靶向B7-H3的ADC候选药物,适用于包括小细胞肺癌、去势抵抗性前列腺癌和食管鳞状细胞癌在内的多种癌症)。
DB-1303采用第三代拓扑异构酶I抑制剂作为有效载荷(P1003),并通过可裂解的肽连接子连接到抗体上。这种设计旨在提高疗效,同时最大限度地减少对健康细胞的损害。DB-1303的药物抗体比率(DAR)约为8。DB-1303/BNT323正在多项临床试验中进行评估,用于治疗晚期/转移性实体瘤,包括乳腺癌和子宫内膜癌。
DB-1303/BNT323具有在HER2阳性和HER2低表达肿瘤中均显示出疗效的潜力。其新型拓扑异构酶I抑制剂有效载荷可能具有旁观者杀伤效应。早期临床试验中观察到的安全性可控。约8的较高药物抗体比率(DAR)可能有助于提高疗效。此外,该药物已获得美国FDA授予的子宫内膜癌治疗快速通道和突破性疗法认定。
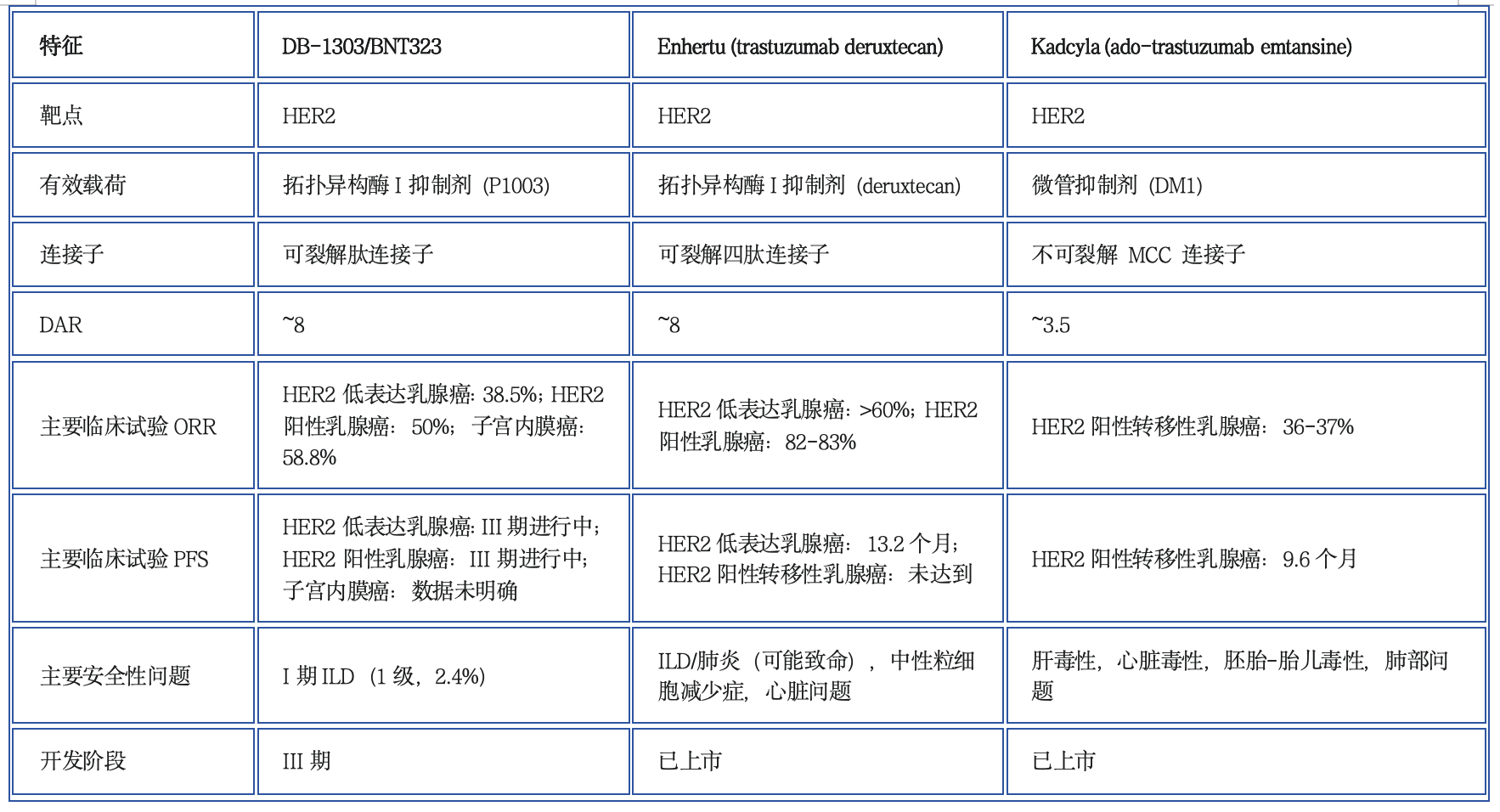
DB-1303/BNT323与同类产品的对比
DB-1311/BNT324靶向B7-H3,B7-H3是一种跨膜糖蛋白,在多种实体瘤中过度表达,包括小细胞肺癌(SCLC)、去势抵抗性前列腺癌(CRPC)和食管鳞状细胞癌(ESCC)。B7-H3在抗肿瘤免疫反应和肿瘤微环境中发挥作用,其过度表达与疾病进展和不良预后相关。这是一个新型且有前景的靶点,已批准的疗法有限。
DB-1311/BNT324目前正在一项全球I/IIa期临床试验(NCT05914116)中进行评估,以评估其在晚期实体瘤患者中的安全性和耐受性。早期临床试验显示出令人鼓舞的抗肿瘤活性,尤其是在SCLC和CRPC中。目前该药物已获得FDA授予的晚期/不可切除或转移性CRPC治疗快速通道资格,以及晚期或转移性ESCC治疗孤儿药资格。
DB-1311/BNT324和默克/第一三共的Ifinatamab Deruxtecan均靶向B7-H3并使用拓扑异构酶I抑制剂作为有效载荷。DB-1311/BNT324在SCLC中显示的初步疗效与Ifinatamab Deruxtecan相当。然而,Ifinatamab Deruxtecan用于SCLC的开发阶段更靠前,已进入III期临床。
中国抗体偶联药物市场预计也将经历显著增长,到2030年预计将达到8.6亿美元,2022年至2030年的复合年增长率为36.9%。中国市场的快速增长凸显了其对创新癌症疗法的日益重视。
ADC市场的主要趋势包括癌症发病率的上升推动了对靶向治疗的需求;连接子技术和偶联方法的快速迭代有望开发出更稳定、更有效和更安全的ADC治疗药物;人们越来越关注和采用将抗体偶联药物与其他抗癌药物(如化疗、免疫疗法和靶向疗法)联合使用的联合疗法,以期改善治疗效果;此外,主要市场参与者之间的投资和合作(包括许可协议、共同开发协议和收购)不断增加,进一步推动了该领域的创新和市场扩张。中国正在成为全球ADC市场的重要参与者,在全球ADC管线中占据相当大的份额(超过42%),并且ADC相关的交易显著增加。
全球ADC市场目前由拥有已批准上市ADC产品的知名制药公司主导,如罗氏、第一三共、阿斯利康、辉瑞和吉利德。
其中,阿斯利康和第一三共共同开发和商业化的Enhertu(trastuzumab deruxtecan)是销售额领先的ADC药物,这得益于其在HER2阳性和HER2低表达乳腺癌以及不断扩大的适应症方面的疗效。罗氏的Kadcyla(ado-trastuzumab emtansine)是另一款市场份额显著的成熟ADC药物,尤其是在HER2阳性转移性乳腺癌方面。
中国ADC市场正在涌现出几家积极参与ADC研发的国内公司,包括荣昌生物、恒瑞医药、映恩生物、多禧生物等。这些公司正在开发针对中国患者特定需求的新型ADC药物,并越来越多地参与全球合作。
如映恩生物已经与BioNTech、GSK等建立了合作关系。这些合作不仅为其提供了资金支持,还验证了映恩生物的技术并促进了其获得全球开发和商业化的机会。这种模式表明,中国生物科技公司在全球制药创新生态系统中正扮演着越来越重要的角色。
虽然全球ADC市场目前由少数几家拥有已批准重磅药物的知名药企主导,但大量创新公司的涌现预示着未来竞争格局可能会发生变化。而具有开发卓越疗效、安全性新药的能力,对于在这个日益拥挤的领域中获得市场份额至关重要。
荣昌生物是国内首家成功推出自研ADC产品的公司,其产品包括泰它西普(Telitacicept,RC18),一种用于治疗系统性红斑狼疮(SLE)的创新双靶点生物制剂,以及维迪西妥单抗(Disitamab Vedotin,RC48;Aidexi®),一种靶向HER2的ADC,用于治疗多种癌症。2024年,荣昌生物报告的年度收入为17.2亿元(约合2.4亿美元),这主要得益于其两款核心产品的销售。
恒瑞医药也积极参与抗体偶联药物的开发,其中包括SHR-A1904,这是一种新型ADC,具有优化的药物抗体比率(DAR),靶向Claudin 18.2,用于治疗实体瘤。
映恩生物未来的成功在很大程度上取决于其药物候选物(特别是核心产品DB-1303/BNT323和DB-1311/BNT324)的成功临床开发、监管批准和最终商业化。此外,ADC领域竞争激烈,技术进步迅速,映恩生物需要不断创新才能保持竞争力。

1、公司官网、招股书
2、映恩生物通过港交所上市聆讯 三年亏损近18亿元
3、映恩生物明日上市,暗盘交易大涨80%


文章评论(0)